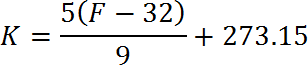Calorimetría y Principios de la Termodinámica
Calorimetría
La calorimetría estudia la transferencia de calor en diferentes procesos. Se distinguen dos casos:
- Si no hay cambio de estado: Q = Ce ⋅ m ⋅ Δt
- Si hay cambio de estado: Q = L ⋅ m
- En mezclas (sistema adiabático): Qganado + Qcedido = 0
Equivalencias:
- 1 Kcal = 1000 cal
- 1 Kcal = 4186 Joule
Definiciones:
- Q: Calor recibido (Cal o Kcal)
- Ce: Calor específico
- m: Masa (kg o g)
- t: Temperatura (°C)
- L: Calor latente
Signo de Q:
- Q > 0: El cuerpo recibió calor (se calentó).
- Q < 0: El cuerpo entregó calor (se enfrió).
Unidades de Ce:
- Cal/g⋅°C
- Kcal/Kg⋅°C
Primer Principio de la Termodinámica
Un sistema termodinámico puede intercambiar energía con su entorno en forma de trabajo y de calor, y acumula energía en forma de energía interna. La relación entre estas tres magnitudes viene dada por el principio de conservación de la energía.
La variación de energía interna (ΔU) de un sistema es igual al trabajo de las fuerzas externas (Wext):

La energía interna coincide con la energía propia, ya que no se considera la traslación del centro de masas del sistema (energía cinética orbital).
El trabajo realizado por el gas (W) es igual y de signo contrario al trabajo de las fuerzas externas. Además, se puede suministrar energía en forma de calor (Q).

La expresión final del primer principio es:

O, de forma equivalente: ΔU = Q – W
Segundo Principio de la Termodinámica y Ciclo de Carnot
El segundo principio de la termodinámica establece que ninguna máquina térmica puede tener un rendimiento del 100%. El ciclo de Carnot proporciona el límite superior de rendimiento para una máquina que opera entre dos focos de temperatura.
Máquina de Carnot
La máquina de Carnot opera en un ciclo reversible que consta de cuatro etapas:
- Expansión isoterma (1-2): El gas absorbe calor Q1 a la temperatura del foco caliente T1.
- Expansión adiabática (2-3): El gas se enfría hasta la temperatura del foco frío T2.
- Compresión isoterma (3-4): El gas cede calor Q2 al foco frío a temperatura T2.
- Compresión adiabática (4-1): El gas se calienta hasta la temperatura del foco caliente T1.

El rendimiento (η) de una máquina de Carnot es:


El rendimiento solo depende de las temperaturas de los focos y siempre es menor que uno.
Refrigerador de Carnot
El ciclo de Carnot, recorrido en sentido inverso, describe un refrigerador. Las etapas son:
- Expansión adiabática (1-2): El gas se enfría hasta T2.
- Expansión isoterma (2-3): El gas absorbe calor Q2 del foco frío a temperatura T2.
- Compresión adiabática (3-4): El gas se calienta hasta T1.
- Compresión isoterma (4-1): El gas cede calor Q1 al foco caliente a temperatura T1.

La eficiencia (ε) de un refrigerador de Carnot es:

Teorema de Carnot
El teorema de Carnot establece que:
Ninguna máquina que opere entre dos focos térmicos puede tener un rendimiento mayor que el de una máquina de Carnot operando entre los mismos focos. Todas las máquinas reversibles que operen entre dos focos poseen el mismo rendimiento, que es el rendimiento de Carnot. |
El rendimiento de Carnot es un límite superior teórico, ya que en la práctica siempre hay irreversibilidades.
Joule y la conservación de la energía: Dentro de los sistemas termodinámicos, una consecuencia de la ley de conservación de la energía es la primera ley de la termodinámica.
Entropía y Procesos Irreversibles
Aunque la energía se conserva, se degrada según la segunda ley de la termodinámica. En procesos irreversibles, la entropía de un sistema aislado aumenta, impidiendo que el sistema vuelva a su estado inicial. La energía se vuelve menos aprovechable. Por ejemplo, la fricción convierte energía mecánica en térmica, y esta última no puede reconvertirse totalmente en mecánica.
Tipos de Vapor
- Vapor húmedo: Vapor que contiene partículas de agua no vaporizadas. Es la forma más común de vapor en plantas industriales.
- Vapor saturado: Vapor en equilibrio con agua líquida a la misma presión y temperatura. Es invisible al salir de una tubería.
- Vapor sobrecalentado: Vapor a una temperatura superior a la de saturación para una presión dada. No se condensa fácilmente y almacena más calor que el vapor saturado.
- Vapor líquido saturado: Es un termino redundante, es lo mismo que vapor saturado.
Fórmulas de Conversión de Temperatura
De Fahrenheit a Celsius
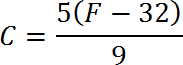
De Celsius a Fahrenheit
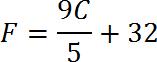
De Kelvin a Celsius
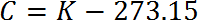
De Celsius a Kelvin
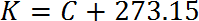
De Kelvin a Fahrenheit
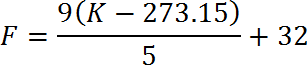
De Fahrenheit a Kelvin